Restrictive vs Liberal Transfusion Strategy in Patients with Acute Brain Injury The TRAIN Randomized Clinical Trial Clincal Trials.gov
ID NCT02968654
Taccone F.S. et al.;JAMA 2024 Oct 9; 332(19):1623-1633;
DOI 10.1001/jama.2024.20424
Correction in JAMA, 2025 Feb 13;333(10):911 (authors name wrong in citations)
Materials and Methods:
Es handelt sich um eine randomisierte multizentrische, Phase-3, Parallelgruppen, Untersucher-initiierte, open-label-Studie, die von 2017 bis 2022 in 72 Intensivstationen in 22 Ländern durchgeführt wurde. Eingeschlossen wurden Patienten mit Hirnverletzung (Schädel-Hirn-Trauma, Subarachnoidalblutung, spontane intrazerebrale Blutung) und einem Alter ≥ 18 Jahre, die innerhalb von 10 Tagen nach Hirnverletzung auf Eignung getestet werden konnten.
Weitere Einschlusskriterien waren GCS ≤ 13, erwarteter Intensivaufenthalt mindestens 72 h und Hämoglobin ≤ 9 g/dl. Die detaillierten Ein- bzw. Ausschlusskriterien entnehmen Sie bitte dem publizierten Studienprotokoll.
Intervention:
850 Patienten wurden randomisiert entweder einer liberalen G-Transfusionsgruppe (Trigger Hb ≤ 9 g/dl) oder einer restriktiven Transfusionsgruppe (Trigger ≤ 7 g/dl) zugeordnet. Nach der Randomisierung erhielten die Patienten 1 FEK, wenn der Transfusionstrigger erreicht wurde.
Primäres Outcome:
Als primäres Outcome wurde der Anteil der Patienten gemessen, der ein schlechtes Outcome (GOSE 1-5) 180 Tage nach Randomisierung zeigte. GOSE 1-5 wurde gewählt, da die Patienten in diesen Gruppen nicht in der Lage sind, mindestens eine oder mehr Rollen in ihrem normalen Leben nicht zu erfüllen und daher sowohl von der Lebensqualität als auch von ihren sozialen Aktivitäten eingeschränkt sind.
Sekundäre Outcomeparameter schlossen das 28 Tage Überleben, Länge des ITS- und Krankenhausaufenthaltes sowie das Auftreten von Organversagen ein.
Die Kalkulation der Populationsgröße basierte auf einer geschätzten Mortalität von 15 % und einer Rate von schlechtem neurologischem Outcome von 35%. Dies würde eine Gruppengröße von 2095 Patienten bedeuten, um eine statistische Power von 90% zu erreichen. Aufgrund von sehr langsamem Patienteneinschluss wurde die notwendige Patientenzahl zweimal nach unten korrigiert.
Alle statistischen Tests wurden mittels des SPSS-Programms durchgeführt mit den üblichen Grenzen für statistische Signifikanz.
Ergebnisse:
Insgesamt wurden 850 Patienten randomisiert. Von 30 Patienten wurde die Einwilligung im Verlauf zurückgezogen, was zu einer Gesamtpopulation von 820 Patienten mit 397 in der liberalen und 423 in der restriktiven Gruppe führte. Die mittlere Zeitdauer von der Aufnahme bis zur Randomisierung betrug 3 Tage. Die Basisdaten in beiden Gruppen waren vergleichbar.
Für die Auswertung des primären Outcomes waren letztendlich Daten von 806 Patienten vorhanden, von denen sich 393 in die liberale und 413 in die restriktive Gruppe verteilten.
Die Verteilung der Hirnverletzung war wie folgt:

Verteilung der initialen Hämoglobinwerte und mittleren niedrigsten Hämoglobinwerte nach Randomisation
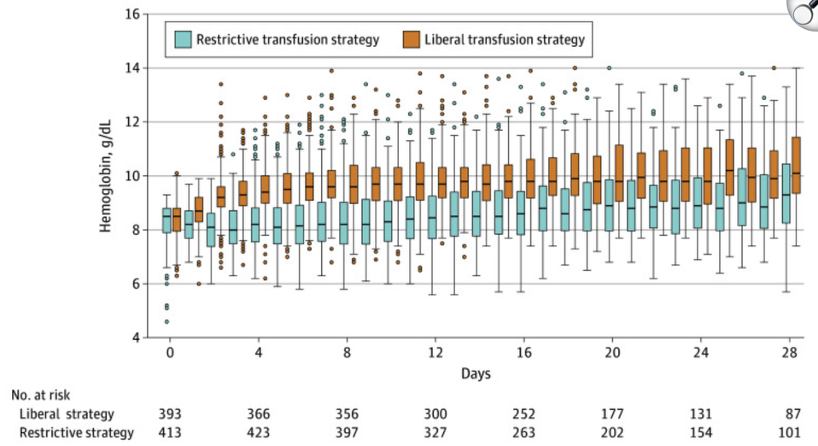
Insgesamt wurden in der liberalen Gruppe 910 Transfusionen bei 357 Patienten (89,9%) vs. 373 Transfusionen bei 205 Patienten (48,5%) in der restriktiven Gruppe durchgeführt p <.001.
Ergebnisse
Der primäre und die sekundären Outcomeparameter zeigten keine statistisch signifikanten Unterschiede zwischen den Gesamtgruppen, allerdings einen Trend zu einem geringeren Auftreten eines schlechten Outcomes in der liberalen Gruppe.
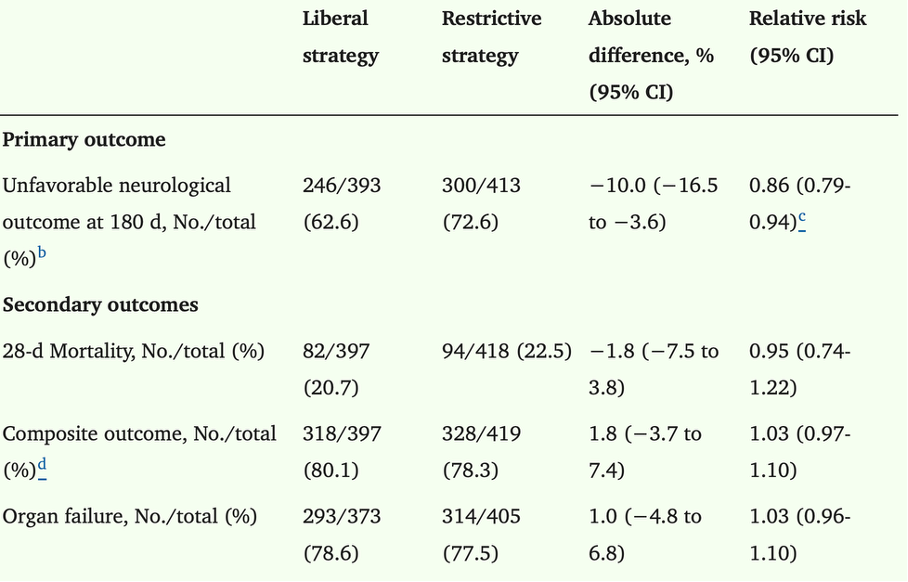
Dieser Trend zeigt sich auch im folgenden Outcomediagramm und auch in der Auflistung der relativen Risiken in den entsprechenden Untergruppen nach Alter, Art der Hirnverletzung, GCS bei Aufnahme etc.
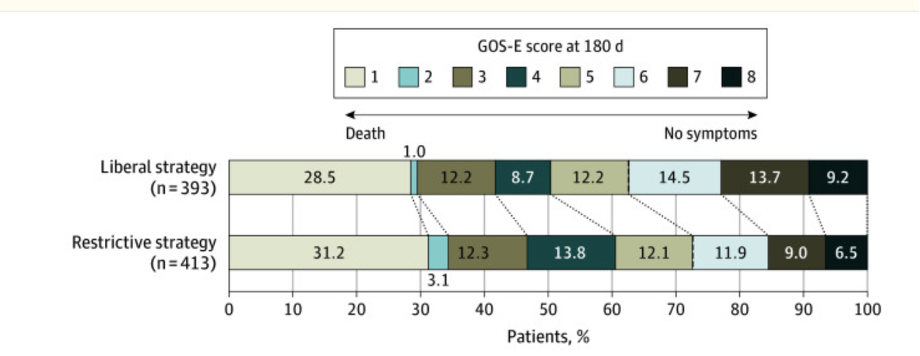
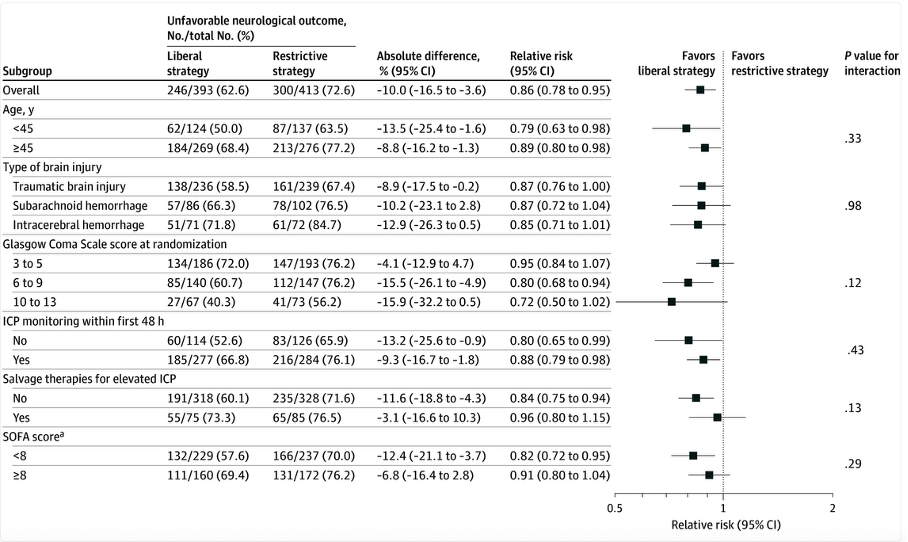
Die Nebenwirkungen waren in beiden Gruppen gleich verteilt. Auffällig war lediglich, dass in der liberalen Gruppe 35/397 Patienten (8,8%) vs. 57/423 (13,5%) in der restriktiven Gruppe mindestens eine zerebrale Ischämie auftrat. Dies war nicht statistisch signifikant.
Diskussion:
Diese Studie zeigt die Tendenz zum besseren neurologischen Outcome sowie zu einer niedrigeren 28-Tage-Mortalität/Organversagensrate bei einem liberalen Transfusionstrigger von ≥9 g/dl bei Patienten mit Hirnverletzung. Trotz deutlich höherer Transfusionsraten kam es zu keinem Unterschied im Auftreten von Adverse Events.
Diese Ergebnisse sind weitgehend konform mit den Ergebnissen der HEMOTION-Studie, stehen allerdings in Widerspruch zu den Daten der SAHaRA-Studie, wobei hier ein anderer Hb-Wert als Trigger verwendet wurde.